A Fisiologia Vegetal
é, em parte, o estudo da água, essencial à
vida.
Muitas atividades da planta são determinadas pelas propriedades
da água e por substâncias dissolvidas na mesma. A
maioria das propriedades peculiares à água se deve
à sua estrutura atômica.
Embora seja eletricamente neutra, a distribuição
assimétrica de seus elétrons torna-a positivamente
carregada de um lado e negativamente do outro. Portanto, a água
é uma molécula dipolo apresentando uma região
positiva e outra negativa (Figura 1).
Dois elétrons não pareados criando uma carga negativa
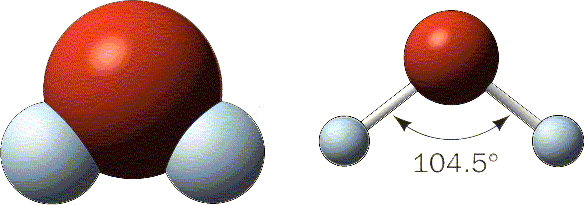
Figura 1.
A molécula de água é formada por um átomo
de oxigênio (bola vermelha) e dois átomos de hidrogênio
(bolas brancas). O modelo estrutural espacial em visualizado
a esquerda enquanto a direita, observa-se o modelo estrutural
do tipo pau-e-bola onde destaca-se a característica polar
da molécula.
A atração
eletrostática da região positiva de uma molécula
pela região negativa de uma outra adjacente induz a formação
de uma ponte de hidrogênio. Embora estas forças
sejam relativamente fracas (aproximadamente 20 KJ mol-1 de pontes
de H) fazem com que as moléculas de água na forma
líquida ou sólida apresentem uma estrutura mais
ou menos ordenada (Figura 2).
Devido à sua polaridade, associada à sua leve
ionização (Figura 1), a água é o
solvente universal: é líquida à temperatura
na faixa biológica normal e seus pontos de fusão
e ebulição são elevados quando comparada
com outras substâncias de tamanho molecular similar, devido
às ligações entre moléculas por
meio das pontes de hidrogênio.
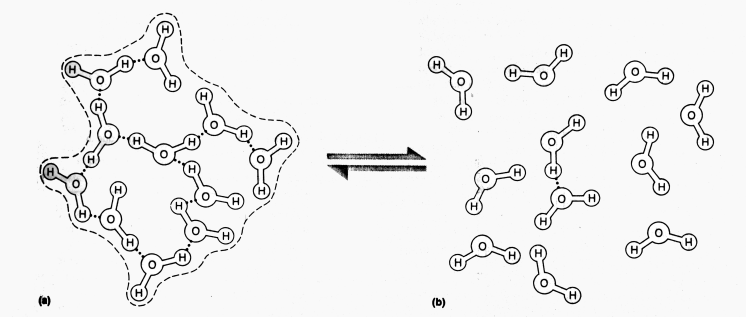
Figura 2. Pontes de hidrogênio entre as moléculas
de água resultam em uma ordenação local
formando uma estrutura quase cristalina (a). Por causa da continua
agitação termal das moléculas de água,
estes agregados locais tem uma vida muito curta, eles se desfazem
rapidamente para formar outras Configurações ao
acaso (b).Caso as pontes de hidrogênio não se formassem,
a água deveria ser gasosa nas temperaturas normais, o
que tornaria a vida na terra inviável. Portanto, a vida
terra somente é possível graças algumas
propriedades físico-químicas da água (Tabela
1).
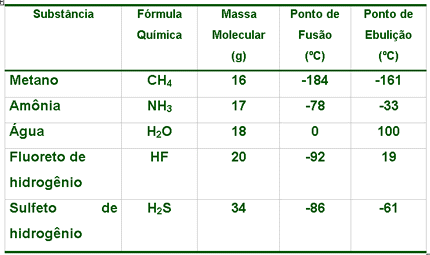
Tabela
1. Algumas propriedades físicas da água em relação
a outras substancias.
Os tecidos
vegetais são altamente hidratados, com teores constituindo
entre 70 e 90% da matéria fresca. Devido ao seu elevado
calor específico existe uma estabilidade térmica
relativamente elevada - órgãos volumosos não
sofrem alterações bruscas de temperatura em resposta
as variações do meio. Entretanto, esta água
não é estacionária, mas está continuamente
em movimento. Por exemplo: a água é evaporada
para atmosfera pela transpiração e reposta pela
absorção através das raízes.
A forma normal das plantas é mantida pela pressão
da água no seu protoplasto pressionando contra as paredes
celulares. O seu crescimento depende da água absorvida
que causa a expansão celular, e o transporte de substâncias
ocorre em meio aquoso.